Sistem imun atau sistem kekebalan adalah sel-sel dan banyak struktur biologis lainnya yang bertanggung jawab atas imunitas, yaitu pertahanan pada organisme untuk melindungi tubuh dari pengaruh biologis luar dengan mengenali dan membunuh patogen. Sementara itu, respons kolektif dan terkoordinasi dari sistem imun tubuh terhadap pengenalan zat asing disebut respons imun. Agar dapat berfungsi dengan baik, sistem ini akan mengidentifikasi berbagai macam pengaruh biologis luar seperti dari infeksi, bakteri, virus sampai parasit, serta menghancurkan zat-zat asing lain dan memusnahkan mereka dari sel dan jaringan organisme yang sehat agar tetap berfungsi secara normal.
Manusia dan vertebrata berahang lainnya memiliki mekanisme pertahanan yang kompleks, yang dapat dibagi menjadi sistem imun bawaan dan sistem imun adaptif. Sistem imun bawaan merupakan bentuk pertahanan awal yang melibatkan penghalang permukaan, reaksi peradangan, sistem komplemen, dan komponen seluler. Sistem imun adaptif berkembang karena diaktifkan oleh sistem imun bawaan dan memerlukan waktu untuk dapat mengerahkan respons pertahanan yang lebih kuat dan spesifik. Imunitas adaptif (atau dapatan) membentuk memori imunologis setelah respons awal terhadap patogen dan membuat perlindungan yang lebih ditingatkan pada pertemuan dengan patogen yang sama berikutnya. Proses imunitas dapatan ini menjadi dasar dari vaksinasi.
Gangguan pada sistem imun dapat berupa imunodefisiensi, penyakit autoimun, penyakit inflamasi, dan kanker. Imunodefisiensi dapat terjadi ketika sistem imun kurang aktif sehingga dapat menimbulkan infeksi berulang dan dapat mengancam jiwa. Pada manusia, imunodefisiensi dapat disebabkan karena faktor genetik seperti pada penyakit defisiensi imunitas kombinasi serta kondisi dapatan seperti sindrom defisiensi imun dapatan (AIDS) yang disebabkan oleh retrovirus HIV. Sebaliknya, penyakit autoimun menyebabkan sistem imun menjadi hiperaktif menyerang jaringan normal seakan-akan jaringan tersebut merupakan benda asing. Di satu sisi, ilmu pengetahuan pun terus berkembang dan manipulasi dalam kedokteran telah dilakukan. Penggunaan obat imunosupresif telah berhasil menekan sistem imun yang hiperaktif, dan penggunaan imunoterapi telah dilakukan untuk pengobatan kanker.
Patogen dapat berevolusi secara cepat dan mudah beradaptasi agar terhindar dari identifikasi dan penghancuran oleh sistem imun, tetapi mekanisme pertahanan tubuh juga berevolusi untuk mengenali dan menetralkan patogen. Bahkan organisme uniseluler seperti bakteri juga memiliki sistem imun sederhana dalam bentuk enzim yang melindunginya dari infeksi bakteriofag. Mekanisme imun lainnya terbentuk melalui evolusi pada eukariota kuno tetapi masih ada hingga sekarang seperti pada tumbuhan dan invertebrata.
A. SEJARAH IMUNOLOGI
Imunologi adalah ilmu yang mempelajari struktur dan fungsi sistem imun. Imunologi awalnya berasal dari ilmu mikrobiologi. Imunitas pertama kali diketahui saat terjadi wabah Athena pada 430 SM. Thukidides mencatat bahwa orang yang sembuh dari penyakit sebelumnya dapat bertahan tanpa terkena penyakit lagi. Lambat laun, diciptakan istilah "immunity" yang diturunkan dari istilah Latin "immunitas" untuk menggambarkan resistensi semacam itu. Pada abad ke-10, dokter Iran Al-Razi merupakan orang pertama yang membedakan antara cacar (smallpox) dan campak (measles) dan juga mencatat kemungkinan teori pertama tentang imunitas dapatan (acquired immunity). Pada abad ke-11, dokter dan filsuf Ibnu Sina juga mengusulkan teori lebih lanjut untuk imunitas dapatan.
Pada sekitar 1000 M, bangsa Tiongkok dilaporkan telah mempraktikkan bentuk imunisasi ini dengan menghirup bubuk kering yang berasal dari kulit lesi cacar. Pada awal abad ke-18 muncul minat baru pada imunitas dapatan melalui penggunaan variolasi sebagai tindakan pencegahan, yaitu dengan memasukkan sebagian dari lesi penderita cacar ke dalam tubuh orang yang sehat. Praktik variolasi juga makin umum dilakukan Inggris pada tahun 1720-an karena usaha Mary Wortley Montagu, istri duta besar Inggris untuk Konstantinopel (sekarang Istanbul), yang mengamati efek positifnya dan melakukannya pada anak-anaknya. Pada tahun 1798 Edward Jenner mempublikasikan hasil vaksinasinya yang pertama, menggunakan nanah dari penderita cacar sapi (cowpox) dan disuntikkan ke seorang anak bernama James Phipps.
Pengamatan imunitas dapatan berikutnya diteliti oleh Louis Pasteur pada tahun 1880 tentang vaksinasi dan pembuktian teori kuman penyakit. Teori tersebut menyatakan bahwa penyakit disebabkan oleh mikroorganisme, dan teori ini merupakan perlawanan dari teori penyakit saat itu, seperti teori miasma yang menyatakan penyakit disebabkan oleh uap atau kabut beracun yang diyakini terdiri dari partikel-partikel dari bahan pembusuk dan dapat diidentifikasi dengan baunya yang busuk. Lebih lanjut, Robert Koch membuktikan teori kuman ini pada 1891, untuk itu ia diberikan penghargaan Nobel pada 1905. Ia membuktikan bahwa mikroorganisme merupakan penyebab dari penyakit infeksi. Virus dikonfirmasi sebagai patogen manusia pada 1901 dengan penemuan virus demam kuning oleh Walter Reed.
Imunologi mengalami perkembangan luar biasa pada akhir abad ke-19 pada penelitian imunitas humoral dan imunitas diperantarai sel. Paul Ehrlich mengusulkan teori rantai samping yang menjelaskan spesifisitas interaksi antigen-antibodi. Kontribusinya dalam memahami imunitas humoral diakui dengan penghargaan Nobel pada 1908, yang bersamaan dengan penghargaan untuk pendiri imunologi seluler, Elie Metchnikoff.
B. PERLINDUNGAN BERLAPIS
Sistem imun tubuh melindungi organisme dari infeksi dengan perlindungan berlapis yang semakin dalam semakin tinggi spesifisitasnya (kekhususannya terhadap jenis infeksi). Pelindung fisik mencegah patogen seperti bakteri dan virus memasuki tubuh. Jika patogen melewati pelindung tersebut, sistem imun bawaan menyediakan perlindungan dengan segera dalam hitungan menit hingga jam. Sistem imun bawaan ditemukan pada semua jenis tumbuhan dan hewan. Jika patogen berhasil melewati respons bawaan, vertebrata memiliki lapisan perlindungan berikutnya yaitu sistem imun adaptif yang diaktifkan oleh respons imun bawaan. Di sini, sistem imun mengadaptasi respons tersebut selama infeksi untuk meningkatkan pengenalan patogen tersebut. Respons ini lalu dipertahankan setelah patogen dimusnahkan dalam wujud memori imunologis sehingga pada kemudian hari sistem imun adaptif dapat melawan patogen yang sama dengan lebih cepat dan efektif.
Sistem imun bawaan dan sistem imun adaptif keduanya memiliki komponen seluler dan humoral, dan masing-masing memberikan imunitas diperantarai sel dan imunitas humoral. Imunitas diperantarai sel diperankan oleh sel-sel imun seperti neutrofil, makrofag, sel NK, dan limfosit, sedangkan imunitas humoral diperankan oleh komponen terlarut seperti antibodi dan protein komplemen. Antibodi adalah protein yang merupakan produk dari sel B yang teraktivasi yang berperan dalam menetralkan patogen dan menginisiasi proses imunologi yang lain seperti pengaktifan sistem komplemen, pengaktifan pembunuhan sel NK, sel T sitotoksik, dan sel-sel efektor lainnya.
| Sistem imun bawaan | Sistem imun adaptif |
|---|---|
| Respons tidak spesifik | Respons spesifik patogen dan antigen |
| Paparan menyebabkan respons maksimal segera | Perlambatan waktu antara paparan dan respons maksimal |
| Komponen imunitas diperantarai sel dan imunitas humoral | Komponen imunitas diperantarai sel dan imunitas humoral |
| Tidak ada memori imunologis | Paparan menyebabkan adanya memori imunologis |
| Ditemukan hampir pada semua bentuk kehidupan | Hanya ditemukan pada vertebrata berahang |
Baik imunitas bawaan dan adaptif bergantung pada kemampuan sistem imun untuk membedakan molekul self dan non-self. Dalam imunologi, molekul self adalah komponen tubuh organisme yang dapat dibedakan dari bahan asing oleh sistem imun. Sebaliknya, molekul non-self adalah yang dianggap sebagai molekul asing. Satu kelas dari molekul non-self adalah antigen (kependekan dari bahasa Inggris antibody generator atau "pembangkit antibodi") yaitu bahan-bahan yang mengikat reseptor imun tertentu dan membangkitkan respons imun.
Bayi yang baru lahir mendapat beberapa lapisan perlindungan pasif yang disediakan oleh ibu. Selama kehamilan, jenis antibodi yang disebut IgG yang dikirim dari ibu ke bayi secara langsung melewati plasenta, sehingga bayi memiliki antibodi tinggi bahkan saat lahir, dengan rentang spesifisitas antigen (fragmen kecil patogen) yang sama dengan ibunya. Air susu ibu atau kolostrum juga mengandung antibodi yang dikirim ke sistem pencernaan bayi dan melindungi bayi terhadap infeksi bakteri sampai bayi dapat menyintesis antibodinya sendiri. Hal ini disebut imunitas pasif karena fetus tidak membuat sel memori atau antibodi sendiri. Pada ilmu kedokteran, imunitas pasif protektif juga dapat dikirim dari satu individu ke individu lainnya melalui serum yang kaya antibodi.
C. SISTEM IMUN BAWAAN
Mikroorganisme atau racun yang berhasil memasuki organisme akan berhadapan dengan mekanisme sistem imun bawaan. Respons bawaan biasanya dijalankan ketika mikrob teridentifikasi oleh reseptor pengenal pola (pattern recognition receptor, PRR) yang mengenali komponen yang disebut pola molekuler terkait patogen (pathogen-associated molecular pattern, PAMP), atau pola molekuler terkait kerusakan (damage-associated molecular pattern, DAMP). Sistem ini tidak memberikan perlindungan yang bertahan lama terhadap serangan patogen, sehingga diperlukan sistem imun lain yaitu sistem imun adaptif. Sistem imun bawaan merupakan sistem dominan pertahanan tubuh pada kebanyakan organisme.
C.1. PENGHALANG PERMUKAAN
Beberapa penghalang melindungi organisme dari infeksi, termasuk penghalang mekanis, kimiawi, dan biologis. Contoh penghalang mekanis yaitu kulit ari tanaman pada daun, eksoskeleton serangga, kulit telur dan membran bagian luar dari telur, serta kulit yang merupakan pertahanan awal terhadap infeksi. Namun, karena organisme tidak dapat sepenuhnya tertutup sempurna dari lingkungan, sistem lainnya diperlukan untuk melindungi tubuh pada bagian seperti paru-paru, usus, dan saluran urogenital. Pada paru-paru, batuk dan bersin secara mekanis mengeluarkan patogen dan iritan lainnya dari saluran pernapasan. Pengeluaran air mata dan urin juga secara mekanis mengeluarkan patogen, sementara ingus dikeluarkan oleh saluran pernapasan dan saluran pencernaan untuk menangkap mikroorganisme.
Penghalang kimiawi juga melindungi tubuh terhadap infeksi. Kulit dan sistem pernapasan mengeluarkan peptida antimikrobial seperti β-defensin. Enzim seperti lisozim dan fosfolipase A2 pada air liur, air mata, dan air susu ibu juga bersifat antibakteri. Sekresi vagina berperan sebagai penghalang kimiawi selama menstruasi pertama, membuat lingkungan vagina agak bersifat asam, sementara semen mengandung defensin dan seng untuk membunuh patogen. Pada lambung, asam lambung dan protease menyediakan pertahanan kimiawi yang sangat kuat untuk melawan patogen yang tertelan.
Flora komensal dalam saluran pencernaan dan saluran urogenital merupakan penghalang biologi yang bersaing dengan patogen untuk makanan dan tempat. Selain itu, flora komensal kadang mengubah kondisi lingkungan mereka seperti pH atau ketersediaan zat besi. Hal ini menyebabkan adanya hubungan simbiosis antara flora komensal dan sistem imun, hingga mengurangi jumlah patogen dan kemungkinan munculnya penyakit. Namun, karena kebanyakan antibiotik menyasar bakteri dan tidak menyerang fungi, antibiotik oral dapat mengakibatkan "pertumbuhan berlebih" dari fungi dan dapat memicu kondisi seperti kandiasis vagina (infeksi jamur pada vagina). Terdapat bukti kuat bahwa konsumsi flora probiotik, seperti kultur murni lactobacillus (umum ditemukan pada yogurt yang belum dipasteurisasi), membantu mengembalikan keseimbangan komposisi mikrob pada usus anak-anak yang terkena infeksi. Hasil penelitian awal juga menunjukkan hal yang serupa dalam kasus gastroenteritis bakterial, radang usus, infeksi saluran kemih, dan infeksi setelah operasi.
C.2. PERADANGAN
Peradangan merupakan salah satu dari respons pertama sistem imun terhadap infeksi. Gejala peradangan yaitu kemerahan, bengkak, dan nyeri yang diakibatkan oleh peningkatan aliran darah ke jaringan. Peradangan dihasilkan oleh senyawa-senyawa eikosanoid dan molekul sitokin, yang dilepaskan oleh sel yang terinfeksi. Senyawa-senyawa eikosanoid, termasuk prostaglandin, menginduksi demam dan pelebaran pembuluh darah, dan leukotrien yang menarik sel darah putih (leukosit). Sitokin juga terlibat, termasuk interleukin yang bertanggung jawab untuk komunikasi antarsel darah putih; kemokin yang mendorong kemotaksis; dan interferon yang memiliki kemampuan antivirus, seperti menghentikan sintesis protein virus yang sedang menginfeksi sel inang. Faktor pertumbuhan dan faktor sitotoksik juga dapat dilepaskan. Sitokin dan senyawa kimia lainnya mengerahkan sel-sel imun ke tempat infeksi dan menyembuhkan jaringan yang mengalami kerusakan yang diikuti dengan pemusnahan patogen.
C.3. SISTEM KOMPLEMEN
Sistem komplemen merupakan kaskade biokimia (rangkaian reaksi berurutan) yang akhirnya menyerang permukaan sel asing. Sistem komplemen terdiri dari lebih dari 20 protein yang berbeda. Sistem ini dinamakan komplemen ("sesuatu yang melengkapi") karena pertama kali kemampuannya dikenali untuk "melengkapi" pembunuhan patogen oleh antibodi. Komplemen merupakan komponen humoral utama dari respons imun bawaan. Banyak spesies memiliki sistem komplemen, termasuk spesies bukan mamalia seperti tumbuhan, ikan, dan beberapa invertebrata.
Pada manusia, respons ini diaktifkan oleh protein komplemen yang terikat ke antibodi yang menempel pada mikrob tersebut atau protein komplemen yang terikat dengan karbohidrat di permukaan mikrob. Sinyal pengenalan ini memicu respons pembunuhan yang cepat. Kecepatan respons ini merupakan hasil dari penguatan yang muncul setelah pengaktifan proteolisis (pemecahan) dari molekul komplemen, yang juga merupakan protease. Setelah protein komplemen terikat pada mikrob, protein-protein ini mengaktifkan aktivitas proteasenya, yang kemudian mengaktifkan protease komplemen lainnya, dan seterusnya. Hasilnya adalah kaskade katalisis yang memperkuat sinyal awal melalui umpan balik positif teratur. Hasil kaskade ini adalah peptida-peptida yang menarik sel-sel imun, meningkatkan permeabilitas pembuluh darah, dan membungkus permukaan patogen (opsonisasi) sehingga menandainya untuk dihancurkan. Protein komplemen yang berkumpul ini juga dapat membunuh sel secara langsung dengan cara merusak membran plasma sel patogen.
C.4. KOMPONEN SELULER
Leukosit (sel darah putih) bertindak layaknya organisme bersel tunggal yang bebas dan merupakan pertahanan penting dalam sistem imun bawaan. Jenis-jenis leukosit dalam sistem imun bawaan di antaranya fagosit (makrofag, neutrofil, dan sel dendritik), sel limfoid bawaan, sel mast, eosinofil, basofil, dan sel NK. Sel-sel tersebut mengidentifikasi dan menghilangkan patogen dengan cara menyerang patogen yang lebih besar melalui kontak atau dengan cara menelan dan lalu membunuh mikroorganisme. Sel-sel pada imunitas bawaan juga merupakan mediator penting pada pengaktifan sistem imun adaptif.
Makrofag, neutrofil, dan sel dendritik merupakan kelas sel sensor yang mendeteksi dan menginisiasi respons imun dengan menghasilkan mediator inflamasi. Sel-sel ini mengekspresikan sejumlah reseptor terbatas untuk mengenali patogen atau sel yang rusak, bernama PRR. Beberapa PRR merupakan reseptor transmembran (reseptor pada permukaan sel), seperti reseptor jenis Toll (Toll-like receptor, TLR) yang dapat mendeteksi struktur pola molekuler terkait patogen (pathogen-associated molecular pattern, PAMP) yang dihasilkan oleh bakteri ekstraseluler atau bakteri yang ditangkap dan mengalami fagositosis. PRR lainnya merupakan protein sitoplasmik (berada di sitoplasma) misalnya reseptor jenis NOD (NOD-like receptor, NLR) yang dapat mendeteksi serangan bakteri intraseluler.
C.4.1. FAGOSIT
Fagositosis adalah sifat penting pada imunitas bawaan yang dilakukan oleh sel fagosit, yaitu sel yang menelan patogen atau partikel. Fagosit biasanya berpatroli di seluruh tubuh mencari patogen, tetapi dapat dipanggil ke lokasi spesifik oleh sitokin. Ketika patogen ditelan oleh fagosit, patogen terperangkap di vesikel intraseluler yang disebut fagosom, yang sesudah itu menyatu dengan vesikel lainnya disebut lisosom untuk membentuk fagolisosom. Patogen dibunuh oleh aktivitas enzim pencernaan atau ledakan pernapasan (respiratory burst) yang mengeluarkan molekul radikal bebas ke fagolisosom. Secara evolusi, fungsi asal fagositosis adalah untuk memperoleh nutrisi, tetapi peran ini diperluas sehingga fagosit juga berfungsi menelan patogen sebagai mekanisme pertahanan. Fagositosis mungkin mewakili bentuk pertahanan tertua, karena fagosit telah diidentifikasikan ada pada vertebrata dan invertebrata.
Neutrofil dan monosit merupakan fagosit utama yang berkeliling di seluruh tubuh untuk mengejar dan menyerang patogen. Neutrofil ditemukan di aliran darah dan merupakan jenis fagosit yang paling melimpah, normalnya sebanyak 50% sampai 60% jumlah leukosit yang bersirkulasi. Selama radang fase akut, terutama karena infeksi bakteri, neutrofil bermigrasi ke tempat radang dalam sebuah proses yang disebut kemotaksis, dan merupakan sel pertama yang tiba pada saat infeksi.
Makrofag merupakan sel serba guna yang bermukim pada jaringan dan menghasilkan banyak zat-zat kimia termasuk enzim, protein komplemen, dan sitokin. Makrofag juga bertindak sebagai "sel pemakan" yang membersihkan tubuh dari sel mati dan debris (pecahan komponen sel) lainnya, dan sebagai sel penyaji antigen yang mengaktifkan sistem imun adaptif.
C.4.2. SEL DENDRITIK
Sel dendritik adalah fagosit pada jaringan yang berhubungan dengan lingkungan luar; oleh karena itu, sel-sel ini terutama berada di kulit, hidung, paru-paru, lambung, dan usus. Mereka dinamai demikian karena kemiripannya dengan dendrit saraf, keduanya memiliki proyeksi seperti paku, tetapi sel dendritik tidak ada hubungan dengan sistem saraf. Sel dendritik menyediakan hubungan antara sistem imun adaptif dan bawaan, dengan cara menyajikan antigen kepada sel T.
C.4.3. SEL PEMBUNUH ALAMI
Sel pembunuh alami (Inggris: Natural Killer, NK) merupakan komponen sistem imun bawaan yang tidak secara langsung menyerang mikrob penyerang. Sebaliknya, sel-sel NK menghancurkan sel-sel inang yang terinfeksi atau sel yang bertransformasi. Sel-sel demikian dinamakan "missing self" ("kehilangan pengenalan diri") dikarenakan sel memiliki penanda permukaan sel (disebut MHC I) yang sangat rendah. Sel NK dinamai "pembunuh alami" karena gagasan awal bahwa mereka tidak memerlukan pengaktifan untuk membunuh sel-sel yang "missing self." Sel-sel tubuh normal tidak dikenali dan tidak diserang oleh sel-sel NK karena mereka mengekspresikan antigen MHC diri yang utuh. Kompleks antigen diri MHC itu dikenali oleh reseptor imunoglobulin sel pembunuh (KIR) yang menahan aktivitas sel NK.
C.4.4. SEL MAST
Sel mast terletak di jaringan penghubung dan membran mukosa, berfungsi untuk mengatur respons peradangan. Mereka berkaitan dengan alergi dan anafilaksis.
C.4.5. GRANULOSIT
Basofil dan eosinofil memiliki kesamaan dengan neutrofil dalam hal adanya banyak granul di sitoplasmanya. Mereka menyekresikan bahan kimia yang ikut serta melindungi tubuh terhadap parasit dan memainkan peran pada reaksi alergi, seperti asma.
C.4.6. SEL LIMFOID BAWAAN
Sel limfoid bawaan (Inggris: innate lymphoid cell, ILC) adalah sekelompok sel imun bawaan yang termasuk dalam garis keturunan limfoid, tetapi tidak memiliki reseptor sel B atau reseptor sel T spesifik antigen. ILC juga tidak mengekspresikan penanda sel myeloid atau dendritik. Kelompok sel ini memiliki fungsi fisiologis yang bervariasi; beberapa fungsi dianalogikan dengan sel T pembantu, sementara kelompok ini juga termasuk sel NK sitotoksik. Oleh karena itu, mereka memiliki peran penting dalam kekebalan protektif dan pengaturan homeostasis dan peradangan, sehingga kelainan pada ILC dapat menyebabkan gangguan sistem imun seperti alergi, asma bronkial, dan penyakit autoimun.
D. SISTEM IMUN ADAPTIF
Sistem imun adaptif berevolusi pada vertebrata awal dan membuat adanya respons imun yang lebih kuat serta terbentuknya memori imunologi, yaitu tiap patogen "diingat" oleh pengenal antigen. Respons imun adaptif bersifat spesifik terhadap antigen tertentu dan membutuhkan pengenalan antigen non-self tertentu selama proses yang disebut presentasi antigen. Spesifisitas antigen memungkinkan produksi respons yang disesuaikan pada patogen tertentu atau sel tertentu yang terinfeksi patogen. Kemampuan tersebut dipelihara di tubuh oleh "sel memori". Sel-sel memori ini akan segera memusnahkan dengan cepat patogen-patogen yang menginfeksi sel kembali di kemudian hari.
D.1. IMUNITAS DIPERANTAI SEL
Komponen sel utama pada sistem imun adaptif yaitu jenis leukosit khusus yang disebut limfosit. Limfosit T (sel T) dan limfosit B (sel B) merupakan jenis limfosit utama yang berasal dari sel punca hematopoietik pada sumsum tulang. Sel T terlibat dalam respons imun diperantarai sel, sedangkan sel B terlibat dalam respons imun humoral. Baik sel T dan sel B memiliki reseptor yang mengenali target spesifik. Sel T mengenali target non-self seperti patogen, tetapi hanya jika antigen telah diolah dan disajikan pada molekul kompleks histokompatibilitas utama (bahasa Inggris: major histocompatibility complex, disingkat MHC). Sementara itu, reseptor antigen pada sel B, yang merupakan suatu molekul antibodi pada permukaan, dapat mengenali semua patogen tanpa perlu adanya pengolahan antigen. Tiap garis keturunan sel B memiliki antibodi yang berbeda, sehingga kumpulan reseptor antigen sel B yang lengkap mewakili semua antibodi yang dapat diproduksi oleh tubuh.
Awalnya, subtipe sel T dibagi menjadi dua yaitu sel T sitotoksik (sel T pembunuh) dan sel T pembantu. Namun seiring pesatnya penelitian imunologi pada dekade terakhir, banyak ditemukan jenis lain dari limfosit misalnya sel T gamma delta (sel T γδ). Sel T sitotoksik hanya mengenali antigen yang dirangkaikan pada molekul MHC kelas I, sementara sel T pembantu hanya mengenali antigen yang dirangkaikan pada molekul MHC kelas II. Dua mekanisme presentasi antigen tersebut memunculkan peran berbeda dua tipe sel T. Jenis lain sel T yang termasuk subtipe minor yaitu sel T γδ, yang mengenali antigen yang tidak melekat pada molekul MHC.
D.1.1. SEL T SITOTOKSIK
Sel T sitotoksik (Inggris: cytotoxic T lymphocyte, CTL) atau sel T pembunuh merupakan subkelompok dari sel T yang membunuh sel yang terinfeksi virus (dan patogen lainnya), sel-sel yang rusak, atau sel yang tidak berfungsi dengan baik. Sel T sitotoksik diaktifkan ketika reseptor sel T melekat pada antigen spesifik ini dalam sebuah kompleks dengan reseptor MHC kelas I dari sel lainnya. Pengenalan MHC: antigen ini dibantu oleh koreseptor pada sel T yang disebut CD8. Sel T lalu berkeliling ke seluruh tubuh untuk mencari sel yang menyajikan antigen ini pada molekul MHC kelas I. Ketika sel T yang aktif berikatan dengan sel yang demikian, sel T melepaskan protein sitotoksik (seperti perforin) yang dapat membentuk pori pada membran plasma target, membuat ion, air, dan toksin masuk ke dalamnya. Hal ini menyebabkan sel mengalami apoptosis. Sel T sitotoksik penting untuk mencegah replikasi virus. Pengaktifan sel T membutuhkan sinyal pengaktifan antigen/MHC yang sangat kuat dan sinyal pengaktifan tambahan yang disediakan oleh sel T pembantu.
D.1.2. SEL T PEMBANTU
Sel T pembantu (Inggris: T helper cell, Th) mengatur respons imun bawaan dan respons imun adaptif, serta membantu menentukan jenis respons imun pada patogen khusus. Sel tersebut tidak memiliki aktivitas sitotoksik dan tidak membunuh sel yang terinfeksi atau membersihkan patogen secara langsung, tetapi mereka mengontrol respons imun dengan mengarahkan sel lain untuk melakukan tugas tersebut.
Sel T pembantu mengekspresikan reseptor sel T yang mengenali antigen terikat pada molekul MHC kelas II. MHC:antigen juga dikenali oleh protein CD4 yang penting dalam pengaktifan sel T. Sel T pembantu memiliki ikatan yang lebih lemah dengan MHC: antigen daripada sel T sitotoksik, sehingga pengaktifannya memerlukan lebih banyak ikatan (sekitar 200-300), sementara sel T sitotoksik dapat diaktifkan dengan satu ikatan molekul MHC:antigen dengan reseptor. Pengaktifan sel T pembantu juga membutuhkan durasi pengikatan lebih lama dengan sel yang memiliki antigen. Sel T pembantu yang telah aktif selanjutnya menyekresikan sitokin yang memengaruhi aktivitas banyak jenis sel. Sinyal sitokin yang dihasilkan oleh sel T pembantu memperbesar fungsi mikrobisidal dari makrofag dan aktivitas sel T sitotoksik. Selain itu, pengaktifan sel T pembantu menyebabkan peningkatan molekul yang diekspresikan pada permukaan sel T, seperti CD40 (juga dikenal sebagai CD154), yang menyediakan sinyal stimulasi tambahan yang dibutuhkan untuk mengaktifkan sel B menjadi sel plasma.
D.1.3. SEL T GAMMA DELTA
Sel T gamma delta (sel T γδ) memiliki reseptor sel T alternatif yang berbeda dengan sel T CD4+ dan CD8+ (αβ), serta memiliki ciri yang mirip dengan sel T pembantu, sel T sitotoksik, dan sel NK, sehingga berada pada perbatasan antara sistem imun adaptif dan sistem imun bawaan. Di satu sisi, sel T γδ merupakan komponen dari sistem imun adaptif karena gen reseptor sel T menjalani penataan ulang dan menghasilan diversitas reseptor serta dapat mengembangkan memori. Di sisi lain, beberapa bagian sel ini merupakan komponen sistem imun bawaan karena reseptor sel T atau reseptor NK yang dimilikinya dapat digunakan sebagai PRR. Contohnya sejumlah besar sel T Vγ9/Vδ2 berespons dalam hitungan jam terhadap molekul umum yang diproduksi oleh mikrob, dan jenis sel T Vδ1+ yang khusus hanya ada di epitelium, merespons terhadap sel epitelial yang rusak.
D.2. IMUNITAS HUMORAL
Pada sistem imun adaptif, peran utama imunitas humoral dijalankan oleh antibodi yang dihasilkan oleh sel B. Sel B mengidentifikasi patogen ketika antibodi yang terikat pada permukaan sel B berikatan dengan antigen asing spesifik. Kompleks antigen:antibodi ini ditelan oleh sel B kemudian antigen dipecah menjadi potongan peptida (proteolisis). Selanjutnya sel B menyajikan peptida antigenik pada permukaan molekul MHC kelas II. Kompleks MHC dan antigen ini menarik sel T pembantu yang memiliki kesesuaian dengan antigen, yang selanjutnya melepaskan sitokin dan mengaktifkan sel B. Sel B yang aktif berikutnya berdiferensiasi menjadi sel plasma yang mengeluarkan jutaan antibodi yang mengenali antigen itu. Antibodi tersebut diedarkan pada plasma darah dan limfatik, mengikat patogen dan menandainya untuk dihancurkan oleh pengaktifan komplemen, atau untuk penghancuran oleh fagosit. Antibodi juga dapat menetralkan toksin bakteri atau dengan mengganggu reseptor yang digunakan virus dan bakteri untuk menginfeksi sel.
E. REGULASI FISIOLOGIS
Sistem imun terlibat dalam banyak aspek regulasi fisiologis dalam tubuh. Sistem imun berinteraksi secara intensif dengan sistem lain, seperti sistem endokrin dan saraf. Sistem imun tubuh juga memainkan peran penting dalam perkembangan serta dalam perbaikan jaringan dan regenerasi.
E.1. HORMON
Hormon dapat bertindak sebagai imunomodulator, yaitu mengubah sensitivitas sistem imun. Sebagai contoh, hormon seks wanita diketahui menstimulasi baik respons imun adaptif dan respons imun bawaan. Beberapa penyakit autoimun seperti lupus erythematosus sering menyerang wanita, dan mulainya serangan sering dengan pubertas. Sebaliknya, hormon seks pria seperti testosteron tampak menekan sistem imun.
E.2. VITAMIN D
Saat suatu sel T menjumpai patogen asing, pada beberapa kasus melibatkan reseptor vitamin D. Hal ini pada dasarnya merupakan alat pensinyalan yang memungkinkan sel T untuk berikatan dengan bentuk aktif vitamin D, suatu hormon steroid kalsitriol. Di sisi lain, sel T mengekspresikan CYP27B1, suatu enzim yang bertanggung jawab mengubah versi pra-hormon vitamin D, kalsidiol, menjadi versi hormon steroid, kalsitriol. Setelah mengikat dengan kalsitriol, sel T dapat melakukan fungsi yang diinginkan. Sel-sel sistem imun lainnya seperti sel dendritik, keratinosit, dan makrofag dikenal mengekspresikan CYP27B1 dan dengan demikian dapat mengaktifkan vitamin D kalsidiol.
Diperkirakan bahwa penurunan progresif kadar hormon seiring bertambahnya usia juga menjadi salah satu faktor yang mengakibatkan pelemahan respons imun pada individu yang menua. Penurunan fungsi kekebalan yang sehubungan dengan usia juga terkait dengan penurunan kadar vitamin D pada lansia. Seiring bertambahnya usia, ada dua hal yang secara negatif memengaruhi kadar vitamin D mereka. Pertama, mereka yang tinggal di dalam rumah akan lebih menurun tingkat aktivitasnya. Mereka mendapat lebih sedikit sinar matahari dan karenanya menghasilkan lebih sedikit kolekalsiferol melalui radiasi ultraungu B. Kedua, seiring bertambahnya usia, kulit menjadi berkurang kemampuannya memproduksi vitamin D.
E.3. TIDUR DAN ISTIRAHAT
Sistem imun bertambah dengan tidur dan beristirahat, sebaliknya kurang tidur dapat merusak fungsi kekebalan tubuh. Putaran umpan balik melibatkan sitokin seperti interleukin-1 dan TNF alfa yang diproduksi sebagai respons terhadap infeksi, tampaknya juga berperan dalam pengaturan tidur non-REM (non-rapid eye movement). Dengan demikian respons imun terhadap infeksi dapat menyebabkan perubahan pada siklus tidur, termasuk peningkatan tidur gelombang lambat relatif terhadap tidur REM.
E.4. NUTRISI DAN DIET
Kelebihan gizi dikaitkan dengan penyakit seperti diabetes dan obesitas, yang diketahui memengaruhi fungsi kekebalan tubuh. Malnutrisi yang lebih sedang, serta defisiensi mineral dan nutrisi tertentu, juga dapat membahayakan respons imun. Demikian juga, kekurangan gizi pada janin dapat menyebabkan kerusakan sistem kekebalan seumur hidup.
E.5. PERBAIKAN DAN REGENERASI
Sistem imun tubuh, khususnya sistem imun bawaan, memainkan peran yang menentukan dalam perbaikan jaringan setelah cedera. Komponen kunci termasuk makrofag dan neutrofil, juga komponen seluler lainnya termasuk sel T γδ, sel limfoid bawaan (ILC), dan sel T regulator (Treg). Makrofag memainkan peran dominan dalam pemulihan homeostasis jaringan dengan membersihkan pecahan komponen seluler (debris sel), renovasi matriks ekstraseluler (extracellular matrix, ECM), dan penyintesisan berbagai sitokin dan faktor pertumbuhan. Dalam konteks penyembuhan jaringan, sel T γδ epitel dendritik (dendritic epithelial γδT cell, DETC) merupakan bagian sel yang sudah dikarakterisasi dengan baik. DETC memiliki morfologi seperti sel dendritik pada kulit tikus, dan mereka merespons dalam beberapa jam terhadap kerusakan jaringan kulit dengan mengeluarkan kemokin dan TNF-α untuk menarik makrofag. Selain itu, DETC mempercepat perbaikan jaringan dengan mensekresi faktor pertumbuhan dan sitokin seperti IGF-1, KGF-1 (FGF-7), KGF-2 (FGF-10), IL-22, dan IL-17A. Plastisitas sel-sel imun dan keseimbangan antara sinyal pro-inflamasi dan anti-inflamasi merupakan aspek penting dari perbaikan jaringan yang efisien.
F. GANGGUAN PADA IMUNITAS
Sistem imun merupakan struktur yang luar biasa efektif dalam hal spesifisitas, indusibilitas, dan adaptasi. Namun, kegagalan pertahanan bisa juga terjadi dan dibagi menjadi tiga kelompok besar: imunodefisiensi, autoimunitas, dan hipersensitivitas.
F.1. IMUNODEFISIENSI
Imunodefisiensi terjadi ketika satu atau lebih komponen sistem imun tidak aktif. Kemampuan sistem imun untuk merespons patogen berkurang pada anak-anak dan orang tua, pada kasus orang tua disebabkan oleh imunosenesens. Di negara-negara berkembang, penyebab melemahnya sistem imun yaitu obesitas, penyalahgunaan alkohol, dan penggunaan obat. Namun, malnutrisi adalah penyebab paling umum yang menyebabkan imunodefisiensi di negara berkembang. Diet dengan protein yang tidak mencukupi dikaitkan dengan gangguan imunitas seluler, aktivitas komplemen, fungsi fagosit, konsentrasi antibodi IgA, dan produksi sitokin. Selain itu, ketiadaan timus pada usia dini melalui mutasi genetik atau pengangkatan melalui operasi mengakibatkan imunodefisiensi yang parah dan kerentanan tinggi terhadap infeksi.
Imunodefisiensi juga bisa muncul akibat faktor turunan atau perolehan (didapat). Penyakit granuloma kronis, yaitu penyakit dengan rendahnya kemampuan fagosit untuk menghancurkan patogen, adalah contoh dari imunodefisiensi turunan. Sementara itu, AIDS dan beberapa jenis kanker merupakan contoh imunodefisiensi dapatan.
F.2. AUTOIMUNITAS
Autoimunitas adalah respons imun terlalu aktif termasuk fungsi imun yang tidak berfungsi baik sehingga berakhir pada gangguan autoimun. Sistem imun tidak mampu membedakan dengan tepat antara self dan non-self, sehingga dapat menyerang bagian dari tubuh. Pada keadaan kondisi yang normal, banyak sel T dan antibodi bereaksi dengan peptida self. Terdapat sel khusus (terletak di timus dan sumsum tulang) yang menyajikan limfosit muda dengan antigen self yang dihasilkan pada tubuh dan untuk membunuh sel yang dianggap antigen self, akhirnya mencegah autoimunitas. Beberapa contoh penyakit autoimun yaitu artritis rematoid, diabetes melitus tipe 1, penyakit Hashimoto, dan lupus eritematosus sistemik.
F.3. HIPERSENSITIVITAS
Hipersensitivitas adalah respons imun yang berlebihan yang dapat merusak jaringan tubuh sendiri. Hipersensitivitas terbagi menjadi empat kelas (Tipe I – IV) berdasarkan mekanisme yang ikut serta dan lama waktu reaksi hipersensitif. Hipersensitivitas tipe I atau reaksi segera atau reaksi anafilaksis sering dikaitkan dengan alergi. Gejala dapat bervariasi dari ketidaknyamanan sampai kematian. Hipersensitivitas tipe I diperantarai oleh IgE, yang memicu degranulasi sel mast dan basofil saat IgE berikatan silang dengan antigen. Hipersensitivitas tipe II terjadi saat antibodi mengikat antigen sel inang dan menandai mereka untuk penghancuran. Jenis ini juga disebut hipersensitivitas sitotoksik, dan diperantarai oleh antibodi IgG dan IgM. Kompleks imun (kompleks antara antigen, protein komplemen dan antibodi IgG dan IgM) terkumpul pada berbagai jaringan yang memicu reaksi hipersensitivitas tipe III. Hipersensitivitas tipe IV (dikenal juga sebagai hipersensitivitas diperantarai sel atau hipersensitivitas jenis tertunda) biasanya membutuhkan waktu antara dua sampai tiga hari untuk berkembang. Reaksi tipe IV ikut serta dalam berbagai penyakit autoimun dan penyakit infeksi, tetapi juga dalam ikut serta dalam dermatitis kontak (misalnya disebabkan oleh racun tumbuhan jelatang). Reaksi tersebut diperantarai oleh sel T, monosit, dan makrofag.
G. MANIPULASI PADA KEDOKTERAN
Respons imun dapat dimanipulasi untuk menekan respons yang tidak diinginkan akibat autoimunitas, alergi, atau penolakan transplantasi. Manipulasi juga dapat dilakukan untuk merangsang respons perlindungan terhadap patogen yang sebagian besar menghindari sistem imun (lihat imunisasi) atau kanker.
G.1. OBAT IMUNOSUPRESIF
Obat imunosupresif digunakan untuk mengontrol gangguan autoimun atau inflamasi ketika terjadi kerusakan jaringan yang berlebihan, dan untuk mencegah penolakan transplantasi setelah transplantasi organ.
Obat anti-inflamasi sering digunakan untuk mengontrol pengaruh peradangan. Glukokortikoid merupakan obat anti-inflamasi yang paling kuat, tetapi obat tersebut memiliki banyak efek samping seperti obesitas pusat, hiperglikemia, dan osteoporosis sehingga penggunaan obat tersebut harus diawasi dengan baik. Obat anti-inflamasi dosis rendah sering digunakan bersamaan dengan obat sitotoksik atau obat imunosupresif seperti metotreksat atau azatioprin. Obat sitotoksik menghambat respons imun dengan membunuh sel yang membelah dengan cepat seperti sel T yang teraktivasi. Namun, pembunuhan sel dilakukan sembarangan sehingga sel-sel membelah dengan cepat lainnya, serta organ-organ lain pun terpengaruh, yang dapat menyebabkan efek samping berbahaya. Obat imunosupresif seperti siklosporin mencegah sel T dari merespons sinyal dengan menghalangi transduksi sinyal.
G.2. IMUNOSTIMULAN
Pada pengobatan tradisional, beberapa obat-obatan tradisional dipercaya dapat menstimulasi imunitas, seperti ekinasea, akar manis, ginseng, astragalus, saga, bawang putih, sangitan, jamur shiitake, jamur lingzhi, hisop, dan madu. Penelitian telah menunjukan bahwa bahan-bahan tersebut dapat menstimulasi sistem imun, walaupun cara kerja mereka belum sepenuhnya dimengerti.
G.3. IMUNOMODULASI (Memodulasi Sistem Imun)
Imunomodulasi adalah modulasi (pengaturan-pengaturan) dari sistem kekebalan. Itu memiliki bentuk alami dan buatan manusia, dan dengan demikian kata tersebut dapat merujuk pada yang berikut :
- Homeostasis dalam sistem kekebalan, di mana sistem mengatur sendiri seperti punya kecerdasan (self-regulation automatically) untuk menyesuaikan respons imun ke tingkat adaptif daripada maladaptif (menggunakan sel T pengatur, molekul pensinyalan sel, dan sebagainya). Di mana molekul pensinyalan berperan penting agar mengenali patogen, kanker atau benda asing yang membahayakan sistem pertahanan tubuh namun tidak menyerang sel-sel normal.
- Imunomodulasi sebagai bagian dari imunoterapi, di mana respons imun diinduksi, diperkuat, dilemahkan, atau dicegah sesuai dengan tujuan terapeutik.
- Imunomodulasi mencakup semua intervensi terapeutik yang bertujuan untuk mengubah respons imun.
Peningkatan respon imun diperlukan untuk mencegah infeksi pada keadaan imunodefisiensi, untuk melawan infeksi yang sudah ada dan untuk melawan kanker. Dalam imunodefisiensi, pengobatan penyebabnya adalah yang paling penting (mis., Malnutrisi, HIV). Cacat kekebalan tertentu jarang dapat diperbaiki, dan pembentukan sistem kekebalan baru dengan transplantasi sel induk alogenik harus dipertimbangkan. Untuk mencegah infeksi, vaksinasi adalah teknik imunomodulator yang paling efektif. Alat baru untuk memanipulasi respons terhadap vaksin melibatkan penggunaan sitokin, vektor virus, dan bahkan "DNA telanjang". Untuk pengobatan infeksi yang sudah mapan, upaya untuk menggeser respon imun ke arah fenotipe tipe Th1 diinginkan. Untuk pengobatan kanker, upaya difokuskan terutama pada menjadikan kanker sebagai target pilihan sistem kekebalan pasien. Untuk efek ini, berbagai pendekatan telah digunakan, termasuk sitokin, anti-CTL-4, antibodi spesifik tumor dan terapi seluler menggunakan limfosit infiltrasi tumor dan bahkan transplantasi sel induk.
Pada alergi, autoimunitas dan transplantasi organ tujuannya adalah untuk melemahkan respon imun. Alergi tertentu dapat diobati dengan desensitisasi tertentu. Dalam autoimunitas dan transplantasi, obat-obatan yang menumpulkan semua respon imun sering digunakan. Berbagai obat dengan target berbeda digunakan sendiri dan dalam kombinasi untuk menginduksi imunosupresi. Agen-agen ini mengganggu presentasi antigen (anti-CD 154, CTLA4-Ig), aktivasi sel-T (penghambat kalsineurin, termasuk siklosporin A dan takrolimus), atau proliferasi sel-T (sirolimus, mycophenolate mofetil, leflunomide). Kortikosteroid bekerja pada beberapa tingkat respons imun dan juga memiliki sifat anti-inflamasi yang signifikan. Obat-obatan ini diperlukan dalam transplantasi organ padat untuk mencegah penolakan, atau mengobatinya jika terjadi. Ketika penolakan berlanjut meskipun telah menggunakan agen penekan imun, cangkok akan hilang dan diperlukan organ baru. Dalam transplantasi sel punca, ekuivalen penolakannya adalah penyakit cangkok vs inang, suatu kondisi patologis di mana sistem kekebalan yang baru didapat mengenali penerima sebagai penerima sebagai benda asing dan meningkatkan respons imun terhadapnya. Ketika penyakit graft vs host tidak merespon steroid, pilihan pengobatan sangat terbatas dan prognosisnya buruk.
G.4. IMUNOLOGI TUMOR
Peran penting sistem imun lainnya yaitu untuk menemukan dan menghancurkan tumor melalui mekanisme yang disebut pengawasan imun (immune surveillance). Sel tumor mengekspresikan antigen yang tidak ditemukan pada sel normal. Oleh sistem imun, antigen tersebut dianggap sebagai antigen asing dan keberadaannya mendorong sel imun untuk menyerang sel tumor tersebut. Antigen yang diekspresikan oleh tumor dapat berasal dari berbagai sumber, misal dari virus onkogenik seperti papillomavirus yang menyebabkan kanker leher rahim, sementara lainnya adalah protein organisme itu sendiri yang diekspresikan pada tingkat tinggi dibanding tingkat pada sel normal sehat. Salah satu contoh yaitu enzim tirosinase yang ketika diekspresikan pada tingkat tinggi, mengubah beberapa sel kulit (seperti melanosit) menjadi tumor yang disebut melanoma. Sumber antigen tumor yang ketiga adalah protein yang secara normal penting untuk mengatur pertumbuhan dan daya hidup sel, tetapi protein ini mengalami mutasi menjadi kanker dan lalu menimbulkan molekul-molekul yang disebut onkogen.
Respons utama sistem imun terhadap tumor yaitu untuk menghancurkan sel abnormal menggunakan sel T sitotoksik, kadang-kadang dengan bantuan sel T pembantu. Antigen tumor disajikan pada molekul MHC kelas I dengan cara yang serupa dengan antigen virus, sehingga sel T sitotoksik dapat mengenali sel tumor sebagai sel abnormal. Sel NK juga membunuh sel tumor dengan cara yang mirip, terutama jika sel tumor memiliki molekul MHC kelas I lebih sedikit pada permukaan daripada keadaan normal; hal ini merupakan fenomena umum pada tumor. Terkadang antibodi dihasilkan untuk melawan sel tumor dan menghancurkannya melalui kerja sama dengan sistem komplemen.
Makrofag memiliki peran ganda dalam karsinogenesis (proses perkembangan kanker). Peran tersebut yaitu dengan cara melawan aktivitas sitotoksik sel imun terhadap sel kanker atau dengan meningkatkan respons antitumor. Makrofag terkait tumor (tumor-associated macrophage, TAM) dapat menghasilkan sitokin dan faktor pertumbuhan seperti TNF-alfa yang dapat memelihara perkembangan tumor atau mendorong plastisitas sifat seperti sel punca. Sementara itu, sel tumor yang terus menerus terpapar keadaan hipoksia relatif ditambah dengan sitokin dan TNF-alfa menyebabkan turunnya produksi protein yang menghalangi metastasis sehingga mempercepat penyebaran sel kanker.
Beberapa tumor menghindari sistem imun dan terus berkembang sampai menjadi kanker. Sel tumor sering memiliki jumlah molekul MHC kelas I yang lebih rendah, sehingga dapat menghindari deteksi oleh sel T sitotoksik. Beberapa sel tumor juga mengeluarkan produk yang mencegah respons imun; contohnya dengan menyekresikan sitokin TGF-β, yang menekan aktivitas makrofag dan limfosit. Selain itu, toleransi imunologis dapat berkembang terhadap antigen tumor sehingga sistem imun tidak lagi menyerang sel tumor.
G.5. MEMORI IMUNOLOGI DAN VAKSINASI
Ketika limfosit telah aktif dan mulai melakukan replikasi, beberapa dari keturunan mereka menjadi sel memori berumur panjang. Sel memori akan mengingat setiap patogen yang pernah ditemui secara spesifik dan dapat melakukan respons lebih kuat jika patogen terdeteksi kembali. Hal ini disebut "adaptif" karena terjadi sepanjang hidup suatu individu dalam beradaptasi pada infeksi patogen dan menyiapkan sistem imun untuk tantangan berikutnya.
Lama waktu respons imun dimulai dengan pertemuan dengan patogen awal (atau vaksinansi awal), dan mendorong pembentukan dan penjagaan memori imunologi aktif.
Memori aktif jangka panjang didapat setelah terjadinya infeksi melalui proses pengaktifan sel B dan sel T. Imunitas aktif dapat juga dibuat melalui vaksinasi. Prinsip di balik vaksinasi (juga disebut imunisasi) yaitu untuk memperkenalkan antigen dari patogen untuk menstimulasi sistem imun dan mengembangkan imunitas spesifik melawan patogen tanpa menyebabkan penyakit yang berkaitan dengan organisme tersebut. Induksi respons imun yang disengaja ini berhasil karena memanfaatkan spesifisitas alami sistem imun. Penyakit infeksi masih menjadi salah satu penyebab utama kematian pada populasi manusia, sehingga vaksinasi muncul sebagai manipulasi sistem imun manusia yang paling efektif.
Kebanyakan vaksin virus berasal dari virus yang dilemahkan, sedangkan banyak vaksin bakteri berasal dari komponen aseluler dari mikroorganisme, termasuk komponen toksin yang tidak berbahaya. Karena banyak antigen berasal dari vaksin aseluler tidak menginduksi respons adaptf dengan kuat, maka kebanyakan vaksin bakteri disediakan dengan penambahan adjuvan yang mengaktifkan sel penyaji antigen pada sistem imun bawaan dan memaksimalkan imunogenisitas.
G.6. PREDIKSI IMUNOGENISITAS
Obat-obat berukuran besar (>500 Da) dapat memicu aksi penetralan oleh respons imun, terutama jika obat digunakan berulang-ulang atau pada dosis yang lebih besar. Hal ini membatasi obat-obat yang berbentuk peptida dan protein dengan ukuran besar (yang umumnya lebih besar dari 6000 Da). Pada beberapa kasus, obat tersebut tidak imunogenik, tetapi dapat diberikan bersamaan dengan senyawa imunogenik, seperti pada kasus paklitaksel ("Taxol") serta kombinasi oksaliplatin dan siklofosfamid.
Metode komputerisasi telah dikembangkan untuk memprediksi imunogenisitas peptida dan protein, yang berguna dalam merancang antibodi untuk obat, menilai keganasan mutasi pada partikel pembungkus virus, dan validasi pengobatan calon obat dengan bahan peptida. Teknik zaman awal memanfaatkan kecenderungan bahwa asam amino hidrofil memiliki konsentrasi lebih tinggi pada daerah epitop. Namun demikian, perkembangan-perkembangan terbaru lebih bersandar pada teknik pembelajaran mesin yang menggunakan basis data epitop yang diketahui ada (biasanya mengenai protein-protein virus yang sudah diteliti dengan baik) sebagai set pelatihan.
Basis data yang dapat diakses publik telah dibuat untuk mengatalogkan epitop dari patogen yang diketahui bisa dikenali oleh sel B. Penelitian berdasarkan bioinformatika terhadap imunogenisitas disebut juga imunoinformatika. Imunoproteomik merupakan studi kumpulan besar protein (proteomika) yang terlibat dalam respons imun.
H. EVALUASI DAN MEKANISME LAINNYA
Sistem imun adaptif dengan berbagai komponennya tampaknya muncul pada vertebrata pertama, sementara invertebrata tidak menghasilkan limfosit atau respons humoral berupa antibodi. Namun, banyak spesies yang memanfaatkan mekanisme-mekanisme yang agaknya merupakan pendahulu imunitas pada vertebrata. Sistem imun pun dimiliki oleh organisme yang paling sederhana, misalnya bakteri menggunakan mekanisme pertahanan unik yang disebut sistem modifikasi restriksi untuk melindungi diri dari patogen virus yang disebut bakteriofag.
Prokariota juga memiliki imunitas adaptif melalui sistem yang menggunakan urutan CRISPR untuk mempertahankan fragmen genom dari bakteriofag yang pernah ditemui sebelumnya, yang memungkinkan prokariota menghalangi replikasi virus melalui mekanisme sejenis interferensi RNA. Sistem imun yang bersifat menyerang juga terdapat pada eukariota uniseluler, tetapi belum banyak penelitian tentang peranan sistem tersebut dalam pertahanan.
Reseptor pengenal pola merupakan protein yang digunakan oleh hampir semua organisme untuk mengidentifikasi molekul yang terkait dengan patogen. Peptida antimikrobial yang disebut defensin adalah komponen evolusioner respons imun bawaan yang ditemukan pada semua jenis hewan dan tumbuhan, serta mewakili bentuk utama imunitas sistemik invertebrata. Sistem komplemen dan fagositik juga digunakan oleh hampir semua bentuk kehidupan invertebrata. Ribonuklease dan jalur interferensi RNA digunakan pada semua eukariot; keduanya diyakini memainkan peran pada respons imun terhadap virus.
Tidak seperti hewan, tumbuhan tidak memiliki sel fagositik, tetapi kebanyakan respons imun tumbuhan melibatkan sinyal kimia bersifat sistemik yang dikirim ke seluruh bagian tumbuhan. Sel-sel tumbuhan merespons molekul yang terkait dengan patogen yang dikenal sebagai pola molekuler terkait patogen (PAMP). Ketika bagian dari tumbuhan terinfeksi, tumbuhan menghasilkan respons hipersensitif, yaitu sel di tempat infeksi mengalami apoptosis dengan cepat untuk mencegah penyebaran penyakit ke bagian lainnya. Resistensi dapatan sistemik merupakan jenis respons pertahanan yang digunakan oleh tumbuhan agar resisten terhadap penyebab infeksi. Mekanisme peredaman RNA sangat penting pada sistem respons sistemik ini karena dapat menghalangi replikasi virus.
H.1. EVALUASI SISTEM IMUN
Sistem imun adaptif dengan berbagai komponennya tampaknya muncul pada vertebrata pertama, sementara invertebrata tidak menghasilkan limfosit atau respons humoral berupa antibodi. Namun, banyak spesies yang memanfaatkan mekanisme-mekanisme yang agaknya merupakan pendahulu imunitas pada vertebrata. Sistem imun pun dimiliki oleh organisme yang paling sederhana, misalnya bakteri menggunakan mekanisme pertahanan unik yang disebut sistem modifikasi restriksi untuk melindungi diri dari patogen virus yang disebut bakteriofag.
Prokariota juga memiliki imunitas adaptif melalui sistem yang menggunakan urutan CRISPR untuk mempertahankan fragmen genom dari bakteriofag yang pernah ditemui sebelumnya, yang memungkinkan prokariota menghalangi replikasi virus melalui mekanisme sejenis interferensi RNA. Sistem imun yang bersifat menyerang juga terdapat pada eukariota uniseluler, tetapi belum banyak penelitian tentang peranan sistem tersebut dalam pertahanan.
Reseptor pengenal pola merupakan protein yang digunakan oleh hampir semua organisme untuk mengidentifikasi molekul yang terkait dengan patogen. Peptida antimikrobial yang disebut defensin adalah komponen evolusioner respons imun bawaan yang ditemukan pada semua jenis hewan dan tumbuhan, serta mewakili bentuk utama imunitas sistemik invertebrata. Sistem komplemen dan fagositik juga digunakan oleh hampir semua bentuk kehidupan invertebrata. Ribonuklease dan jalur interferensi RNA digunakan pada semua eukariot; keduanya diyakini memainkan peran pada respons imun terhadap virus.
Tidak seperti hewan, tumbuhan tidak memiliki sel fagositik, tetapi kebanyakan respons imun tumbuhan melibatkan sinyal kimia bersifat sistemik yang dikirim ke seluruh bagian tumbuhan. Sel-sel tumbuhan merespons molekul yang terkait dengan patogen yang dikenal sebagai pola molekuler terkait patogen (PAMP). Ketika bagian dari tumbuhan terinfeksi, tumbuhan menghasilkan respons hipersensitif, yaitu sel di tempat infeksi mengalami apoptosis dengan cepat untuk mencegah penyebaran penyakit ke bagian lainnya. Resistensi dapatan sistemik merupakan jenis respons pertahanan yang digunakan oleh tumbuhan agar resisten terhadap penyebab infeksi. Mekanisme peredaman RNA sangat penting pada sistem respons sistemik ini karena dapat menghalangi replikasi virus.
H.2. IMUNITAS ADAPTIF ALTERNATIF
Evolusi sistem imun adaptif terjadi pada nenek moyang vertebrata berahang. Banyak molekul klasik pada sistem imun adaptif (seperti antibodi dan reseptor sel T) hanya dimiliki vertebrata berahang. Namun, molekul berbeda yang berasal dari limfosit ditemukan pada vertebrata tak berahang primitif, seperti ikan lamprey dan remang. Hewan tersebut memiliki sejumlah molekul disebut reseptor limfosit variabel, mirip reseptor antigen pada vertebrata berahang, yang dihasilkan dari segelintir gen (satu atau dua). Molekul tersebut dipercaya berikatan pada patogen dengan cara yang sama dengan antibodi dan dengan tingkat spesifisitas yang sama.
H.3. MANIPULASI OLEH PATOGEN
| Peran Mikronutrien | Imunitas bawaan | Imunitas Adaptif |
|---|---|---|
| Vitamin C | Antioksidan efektif yang melindungi terhadap ROS dan RNS dihasilkan ketika patogen dibunuh oleh sel imun. Meregenerasi antioksidan penting lainnya seperti glutathione dan vitamin E ke keadaan aktifnya. Mempromosikan sintesis kolagen, sehingga mendukung integritas penghalang epitel. Merangsang produksi, fungsi dan pergerakan leukosit (misalnya, neutrofil, limfosit, fagosit). Meningkatkan kadar serum protein komplemen. Memiliki peran dalam aktivitas antimikroba dan sel NK dan kemotaksis. Terlibat dalam apoptosis dan pembersihan neutrofil bekas dari tempat infeksi oleh makrofag. | Dapat meningkatkan kadar antibodi serum. Memiliki peran dalam diferensiasi dan proliferasi limfosit |
| Vitamin D | Reseptor vitamin D diekspresikan dalam sel imun bawaan (misalnya, monosit, makrofag, sel dendritik). Meningkatkan diferensiasi monosit menjadi makrofag. Merangsang proliferasi sel kekebalan dan produksi sitokin serta membantu melindungi dari infeksi yang disebabkan oleh patogen 1,25-dihidroksivitamin D3, bentuk aktif vitamin D, mengatur protein antimikroba cathelicidin dan defensin, yang secara langsung dapat membunuh patogen, terutama bakteri. | Terutama efek penghambatan pada imunitas adaptif; misalnya, 1,25-dihidroksivitamin D3 menekan produksi antibodi oleh sel B dan menghambat proliferasi sel T. |
| Vitamin A | Membantu menjaga integritas struktural dan fungsional sel mukosa di penghalang bawaan (misalnya, kulit, saluran pernapasan, dll.). Penting untuk fungsi normal sel imun bawaan (misalnya, sel NK, makrofag, neutrofil) | Diperlukan untuk berfungsinya limfosit T dan B, dan dengan demikian untuk menghasilkan respons antibodi terhadap antigen. Terlibat dalam pengembangan dan diferensiasi sel Th1 dan Th2 dan mendukung respon anti-inflamasi Th2. |
| Vitamin E | Antioksidan penting yang larut dalam lemak. Melindungi integritas membran sel dari kerusakan yang disebabkan oleh radikal bebas. Meningkatkan produksi IL-2 dan aktivitas sitotoksik sel NK. | Meningkatkan fungsi yang dimediasi sel T dan proliferasi limfosit. Mengoptimalkan dan meningkatkan Th1 dan menekan respon Th2. |
| Vitamin B6 | Membantu mengatur peradangan. Memiliki peran dalam produksi sitokin dan aktivitas sel NK. | Diperlukan dalam sintesis endogen dan metabolisme asam amino, bahan penyusun sitokin dan antibodi. Berperan dalam proliferasi, diferensiasi, dan pematangan limfosit. Mempertahankan respons imun Th1. Berperan dalam produksi antibodi. |
| Vitamin B12 | Berperan dalam fungsi sel NK | Dapat berperan sebagai imunomodulator untuk imunitas seluler, terutama dengan efek pada sel sitotoksik (sel NK, sel CD8+ T). Memfasilitasi produksi limfosit T. Terlibat dalam imunitas humoral dan seluler dan metabolisme satu karbon (interaksi dengan folat). |
| Folat | Mempertahankan imunitas bawaan (sel NK). | Berperan dalam imunitas yang diperantarai sel. Penting untuk respon antibodi yang cukup terhadap antigen. Mendukung respon imun yang dimediasi Th 1. |
| Zinc (Seng) | Efek Antioksidan melindungi terhadap ROS dan RNS. Membantu memodulasi pelepasan sitokin dan menginduksi proliferasi sel CD8+ T. Membantu menjaga integritas kulit dan membran mukosa. | Peran sentral dalam pertumbuhan sel dan diferensiasi sel imun yang memiliki diferensiasi dan pergantian yang cepat. Penting untuk pengikatan intraseluler tirosin kinase ke reseptor sel T, diperlukan untuk pengembangan dan aktivasi limfosit T. Mendukung respon Th1. |
| Iron (Besi) | Terlibat dalam regulasi produksi dan aksi sitokin. Membentuk radikal hidroksil yang sangat beracun, sehingga terlibat dalam proses pembunuhan bakteri oleh neutrofil. Penting dalam pembentukan ROS yang membunuh patogen. | Penting dalam diferensiasi dan proliferasi limfosit T. Penting untuk diferensiasi dan pertumbuhan sel, komponen enzim penting untuk fungsi sel kekebalan (misalnya, ribonukleotida reduktase yang terlibat dalam sintesis DNA) |
| Copper (Tembaga) | Pemulung radikal bebas. Sifat antimikroba. Terakumulasi di tempat peradangan, penting untuk produksi dan respons IL-2. Mungkin berperan dalam respon imun bawaan terhadap infeksi bakteri. | Berperan dalam proliferasi sel T. Memiliki peran dalam produksi antibodi dan imunitas seluler. |
| Selenium | Penting untuk fungsi enzim yang bergantung pada selenium (selenoprotein) yang dapat bertindak sebagai regulator redoks dan antioksidan seluler, berpotensi melawan ROS. Selenoprotein penting untuk antioksidan sistem pertahanan host yang mempengaruhi leukosit dan fungsi sel NK. | Terlibat dalam proliferasi limfosit T. Berperan dalam sistem humoral (misalnya, produksi imunoglobulin) |
Meja 2
Defisiensi mikronutrien spesifik pada tahap kehidupan di Eropa. Asupan mikronutrien yang dilaporkan di bawah tunjangan makanan yang direkomendasikan ditampilkan dalam huruf tebal. Tabel juga menunjukkan tingkat asupan atas yang dapat ditoleransi, tingkat asupan nutrisi harian tertinggi yang kemungkinan tidak menimbulkan risiko efek kesehatan yang merugikan pada kebanyakan orang.
| Pilih Mikronutrien | Tunjangan Diet yang Direkomendasikan [ 78 ] | Level Asupan Atas yang Dapat Ditoleransi [ 78 ] | Asupan Mikronutrien Rata-rata yang Dilaporkan, Min – Maks [ 96 ] | ||||||
| Anak - anak 4–8 tahun 9–13 tahun 14–18 tahun: M / F | Dewasa 19–50 tahun: M / F b | Usia tua 51 s / d> 70 tahun: M / F | Anak - anak 4–8 tahun 9–13 tahun 14–18 tahun | Dewasa 19–50 tahun: b | Usia lebih tua 51 s / d> 70 tahun | Anak-anak 4–6 tahun: P / F 7–9 tahun: L / F 10–14 tahun: L / P 15–18 tahun: M / F | Dewasa 19–50 tahun: M / F | Usia tua 51 s / d> 70 tahun: M / F | |
| Vitamin C, mg / hari | 25 45 75/65 | 90/75 | 90/75 | 650 1200 1800/1800 | 2000 | 2000 | 60–157 / 61–157 63–172 / 57–172 73–197 / 77–222 71–201 / 67–205 | 64–153 / 62–153 | 59–142 / 60–160 |
| Vitamin D, μg / hari | 15 | 15 | 15–20 | 75 100 100/100 | 100 | 100 | 1.8–5.8 / 1.5–6.5 1.5–6.4 / 1.5–5.1 1.5–4.8 / 1.2–4.5 1.8–7.5 / 1.5–7.1 | 1.6–10.9 / 1.2–10.1 | 0,7–15,0 / 0,7–12,9 |
| Vitamin A, μg / hari | 400 600 900/700 | 900/700 | 900/700 | 900 1700 2800/2800 | 3000 | 3000 | 400–1100 / 400–1200 400–1300 / 400–1100 400–2400 / 300–2300 400–1800 / 300–1600 | 500–2200 / 500–2000 | 500–2500 / 400–2300 |
| Vitamin E, mg / hari | 7 11 15 | 15 | 15 | 300 600 800 | 1000 | 1000 | 5.3–9.8 / 5.1–9.8 6.3–11.2 / 5.9–13.3 5.9–14.5 / 5.6–18.1 6.8–20.8 / 6.0–15.5 | 3.3–17.7 / 4.2–16.1 | 6.3–13.7 / 6.7–13.7 |
| Vitamin B6, mg / hari | 0,6 1,0 1,3 / 1,2 | 1.3 | 1.7 / 1.5 | 40 60 80 | 100 | 100 | 1.3–1.8 / 1.0–1.9 1.2–2.5 / 1.1–1.9 1.2–2.8 / 1.1–2.7 1.5–3.1 / 1.2–2.5 | 1.6–3.5 / 1.3–2.1 | 1.2–3.0 / 1.2–2.9 |
| Vitamin B12, μg / hari | 1.2 1.8 2.4 | 2.4 | 2.4 | ND | ND | ND | 2.7–5.3 / 2.6–5.0 3.6–5.5 / 2.2–5.3 3.2–11.8 / 2.2–11.1 4.9–7.5 / 3.5–5.2 | 1.9–9.3 / 1.0–8.8 | 3.1–8.2 / 2.5–7.5 |
| Folat, μg / hari | 200 300 400 | 300-400 | 400 | 400 600 800 | 1000 | 1000 | 120–256 / 109–199 144–290 / 133–264 149–428 / 140–360 190–365 / 154–298 | 203–494 / 131–392 | 139–343 / 121–335 |
| Seng, mg / hari | 5 8 11/9 | 11/8 | 11/8 | 12 23 34 | 40 | 40 | 6.0–9.2 / 5.3–8.9 7.0–10.9 / 6.4–9.4 7.0–14.6 / 6.1–13.9 9.3–15.2 / 6.4–11.0 | 8.6–14.6 / 6.7–10.7 | 7.5–12.3 / 6.7–11.2 |
| Besi, mg / hari | 10 8 11/15 | 18/8 | 8 | 40 40 45 | 45 | 45 | 7.3–10.6 / 6.8–10.6 8.4–11.8 / 7.7–11.8 9.2–19.4 / 7.7–14.8 10.2–19.0 / 7.8–14.0 | 10.6–26.9 / 8.2–22.2 | 10.2–25.2 / 8.5–20.9 |
| Tembaga, μg / hari | 440 700 890 | 900 | 900 | 3000 5000 8000 | 10.000 | 10.000 | 700–2200 / 700–2000 900–2800 / 800–2600 800–2900 / 700-2800 1200–3400 / 800–2100 | 1100–2300 / 1000–2200 | 1100–1900 / 900–1900 |
| Selenium, μg / hari | 30 40 55 | 55 | 55 | 150 280 400 | 400 | 400 | 23–61 / 24–61 27–41 / 26–58 29–110 / 28–104 39–59 / 30–38 | 36–73 / 31–54 | 39–62 / 34–55 |
a Meskipun nilai asupan yang memadai disediakan oleh Institute of Medicine untuk bayi (0-12 bulan) dan tunjangan makanan yang direkomendasikan untuk anak-anak (1-3 tahun), ada sedikit data mengenai defisiensi mikronutrien pada kelompok usia ini di negara-negara industri. dan karena itu usia ini tidak dimasukkan dalam tabel ini; nilai b berbeda pada kehamilan dan menyusui. F, perempuan; M, laki-laki; ND, tidak ditentukan.
Tabel 3
Dampak defisiensi mikronutrien dan suplementasi pada respons imun dan risiko infeksi.
| Mikronutrien | Dampak Kekurangan | Dampak Suplementasi |
|---|---|---|
| Vitamin C | Peningkatan kerusakan oksidatif Peningkatan insiden dan keparahan pneumonia dan infeksi lain Penurunan resistensi terhadap infeksi dan kanker, penurunan respon hipersensitivitas tipe tertunda, gangguan penyembuhan luka | Sifat antioksidan melindungi leukosit dan limfosit dari stres oksidatif Lansia: kemungkinan pengurangan insiden dan durasi pneumonia Anak-anak: durasi berkurang dan keparahan gejala flu biasa; hasil yang lebih baik pada gejala pneumonia, malaria dan diare |
| Vitamin D | Peningkatan kerentanan terhadap infeksi, terutama RTI Peningkatan morbiditas dan mortalitas, peningkatan keparahan infeksi, penurunan jumlah limfosit, penurunan berat organ limfoid Peningkatan risiko penyakit autoimun (misalnya, diabetes tipe 1, multiple sclerosis, lupus eritematosus sistemik , rheumatoid arthritis) | Mengurangi infeksi saluran pernapasan akut jika kurang |
| Vitamin A | Mempengaruhi banyak fungsi kekebalan, termasuk jumlah dan aktivitas membunuh sel NK, fungsi neutrofil, kemampuan makrofag untuk fagosit patogen, pertumbuhan dan diferensiasi sel B, penurunan jumlah dan distribusi sel T, dll Peningkatan kerentanan terhadap infeksi (misalnya, diare, RTI, campak, malaria) | Anak-anak: Mengurangi semua penyebab kematian, kejadian diare dan mortalitas, dan kejadian campak dan morbiditas pada anak-anak yang kekurangan (6 bulan sampai 5 tahun); penurunan risiko morbiditas dan mortalitas dari penyakit menular Tidak bermanfaat pada pneumonia |
| Vitamin E. | Defisiensi jarang terjadi pada manusia Merusak aspek imunitas adaptif yang dimediasi oleh sel dan humoral, termasuk fungsi sel B dan T | Lansia: berkurangnya RTI |
| Vitamin B6 | Limfositopenia, mengurangi berat jaringan limfoid, mengurangi respons terhadap mitogen, defisiensi umum dalam imunitas yang dimediasi sel, menurunkan respons antibodi | |
| Vitamin B12 | Respon imun tertekan (misalnya, respon hipersensitivitas tipe tertunda, proliferasi sel T) * | |
| Folat | Respon imun tertekan (misalnya, respon hipersensitivitas tipe tertunda, proliferasi sel T) * | |
| Seng | Penurunan jumlah dan fungsi limfosit, terutama sel T, peningkatan atrofi timus, perubahan produksi sitokin yang berkontribusi terhadap stres oksidatif dan peradangan Meningkatnya infeksi bakteri, virus dan jamur (terutama diare dan pneumonia) [serta morbiditas diare dan pernapasan meningkatan atrofi timus dan risiko infeksi | Pemulihan aktivitas timulin, peningkatan jumlah sel T sitotoksik, pengurangan jumlah sel T helper yang diaktifkan (yang dapat berkontribusi pada autoimunitas), peningkatan sitotoksisitas sel pembunuh alami, pengurangan insiden infeksi Anak-anak: pengurangan durasi diare dan insiden pneumonia pada anak berisiko> 6 bulan, tetapi tidak pada anak 2-6 bulan; mengurangi durasi dan keparahan gejala flu biasa ; hasil yang lebih baik pada gejala pneumonia, malaria dan diare |
| Besi | Berkurangnya kapasitas untuk respon imun yang adekuat (penurunan respon hipersensitivitas tipe tertunda, respon mitogen, aktivitas sel NK), penurunan aktivitas bakterisida limfosit, penurunan level interleukin-6 | Dapat meningkatkan atau melindungi dari infeksi bakteri, virus, jamur dan protozoa tergantung pada tingkat zat besi Secara teoritis dapat meningkatkan kekebalan terhadap penyakit menular, tetapi suplementasi yang tidak tepat sasaran dapat meningkatkan ketersediaan zat besi untuk pertumbuhan patogen dan virulensi serta meningkatkan kerentanan terhadap malaria dan sepsis bakteri khususnya Anak-anak: potensi efek merugikan pada anak-anak yang penuh zat besi |
| Tembaga | Tingkat neutrofil yang sangat rendah Berpotensi meningkatkan kerentanan terhadap infeksi | Anak-anak: peningkatan kemampuan sel darah putih tertentu untuk menelan patogen jika kekurangan Penurunan produksi antibodi sebagai respons terhadap vaksin influenza dengan dosis tinggi kronis pada pria muda yang sehat |
| Selenium | Gangguan imunitas humoral dan seluler Peningkatan virulensi virus Penekanan fungsi kekebalan, peningkatan insiden kanker dan kardiomiopati dengan defisiensi kronis Anak-anak: peningkatan risiko infeksi pernapasan dalam 6 minggu pertama kehidupan | Meningkatkan imunitas yang dimediasi sel dan meningkatkan respon imun terhadap virus pada individu yang kekurangan, tetapi dapat memperburuk asma alergi dan mengganggu respon imun terhadap parasit |
* Efek sistem kekebalan dari defisiensi vitamin B12 dan defisiensi folat secara klinis tidak dapat dibedakan. RTI, infeksi saluran pernafasan.
Mempertimbangkan pentingnya mikronutrien dalam kekebalan, dan fakta bahwa banyak orang dari segala usia memiliki kekurangan mikronutrien tunggal atau ganda yang dapat memiliki efek imunologis yang merugikan, ada alasan untuk suplementasi mikronutrien untuk mengembalikan konsentrasi ke tingkat yang direkomendasikan, terutama setelah infeksi, dan untuk mendukung fungsi dan pemeliharaan kekebalan. Untuk menghindari efek samping yang tidak diinginkan, tentu saja penting untuk memastikan bahwa suplementasi tidak melebihi tingkat asupan atas yang dapat ditoleransi (Meja 2), tingkat asupan nutrisi harian tertinggi yang kemungkinan tidak menimbulkan risiko efek kesehatan yang merugikan pada kebanyakan orang . Meskipun secara teoritis mungkin, data asupan mikronutrien yang dilaporkan dalam format Meja 2 menunjukkan bahwa suplementasi berlebihan tidak mungkin terjadi pada sebagian besar mikronutrien, mungkin dengan pengecualian vitamin A pada anak-anak. Perlu dicatat bahwa margin keamanan dalam suplemen mikronutrien memastikan bahwa konsumsi yang tepat tidak mengakibatkan suplementasi berlebihan, dan label suplemen makanan harus dibaca dengan cermat untuk menghindari penyalahgunaan dan potensi suplementasi berlebihan.
Karena tidak ada biomarker tunggal yang secara akurat mencerminkan efek suplementasi pada respon imun, hasil klinis malah digunakan untuk menentukan efektivitas suplementasi.
I.5.1. BAYI DAN ANAK-ANAK
Defisiensi mikronutrien terkait erat dengan penyakit menular yang dapat menyebabkan morbiditas dan mortalitas yang substansial pada bayi dan anak-anak. Di seluruh dunia, studi suplementasi mikronutrien telah melihat efek vitamin D, A dan E dan mineral seperti besi, selenium dan seng. Suplementasi zinc mengurangi morbiditas dan mortalitas dari penyakit menular pada bayi dan anak-anak di negara berkembang. Pada bayi berat lahir rendah, suplemen zinc sebagian dapat memulihkan imunitas yang dimediasi oleh sel. Seng juga dapat mengurangi risiko dan durasi pneumonia pada anak-anak, membantu mengelola diare pada masa kanak-kanak, menyebabkan lebih sedikit episode malaria, dan mengurangi durasi diare. Pada anak-anak dengan defisiensi vitamin A, suplementasi dapat menurunkan risiko morbiditas dan mortalitas dari penyakit menular. Durasi dan keparahan gejala flu biasa dapat dikurangi dengan suplementasi zinc pada anak-anak ketika dikonsumsi dalam waktu 24 jam setelah onset gejala. Hasil serupa telah diamati dengan vitamin C, yang memperpendek durasi pilek pada anak-anak (terutama dengan dosis yang lebih tinggi) dan mengurangi keparahan gejala; efek yang lebih besar diamati pada anak-anak dibandingkan dengan orang dewasa, termasuk efek profilaksis yang lebih besar dari vitamin C. Seng dan vitamin C juga dapat meningkatkan hasil dari pneumonia, malaria dan infeksi diare pada anak-anak, dan mengurangi kejadian diare dan campak.
I.5.2. REMAJA DAN DEWASA
Suplementasi dengan vitamin C mengurangi durasi dan keparahan gejala flu biasa pada orang dewasa. Pada mereka yang mengalami stres fisik (misalnya, di tempat kerja, selama olahraga, dan di bawah suhu ekstrim), atau dalam kasus di mana kadar vitamin C sedikit di bawah tingkat yang disarankan, suplementasi vitamin C mengurangi kejadian flu biasa. Sebagai contoh, pada pria muda dengan kekurangan vitamin C marginal, suplementasi terbukti mengurangi kejadian flu biasa dan durasi gejala flu dibandingkan dengan plasebo, disertai dengan peningkatan tingkat aktivitas. Ketika digunakan dalam kombinasi dengan seng, suplementasi vitamin C dapat meredakan gejala seperti rinore pada flu biasa, yang umumnya dianggap sebagai gejala infeksi yang paling sering dan menyusahkan (bersama dengan hidung tersumbat). Suplementasi dengan vitamin D dapat melindungi dari infeksi saluran pernafasan dan mengurangi resiko penyakit pernafasan akut dan influenza, terutama dengan dosis sekali sehari. Manfaat sangat jelas terlihat pada mereka yang sangat kekurangan vitamin D. Mengingat efek positifnya pada infeksi saluran pernapasan, telah disarankan bahwa ada alasan yang baik untuk menggabungkan vitamin C dan D dengan seng untuk mendukung fungsi kekebalan dan membantu meminimalkan risiko infeksi. Suplementasi dengan beberapa mikronutrien memiliki efek menguntungkan pada gejala yang terkait dengan apa yang disebut "sindrom gedung sakit", terkait dengan kontak lama dengan faktor lingkungan yang bertindak sebagai kendaraan untuk polutan. Secara signifikan lebih sedikit orang dewasa yang menerima suplemen mikronutrien melaporkan sakit kepala, sakit mata, hidung tersumbat, radang tenggorokan, kelelahan / nyeri, diare atau gejala yang berhubungan dengan infeksi saluran pernapasan akut, seperti batuk.
I.5.3. ORANG YANG LEBIH TUA
Imunitas yang terganggu pada orang tua, sering disebabkan oleh defisiensi mikronutrien multipel, terbukti dalam peningkatan insiden dan keparahan infeksi umum yang mempengaruhi saluran pernapasan atas dan bawah, serta saluran kemih dan genital. Suplementasi dengan jumlah sederhana dari kombinasi mikronutrien dapat memiliki efek menguntungkan. Tingkat sel CD4 + dan CD8 + T yang lebih tinggi dan peningkatan respon proliferasi limfosit terhadap mitogen telah diamati dengan suplementasi vitamin A, C dan E, sementara suplementasi mikronutrien dengan tingkat vitamin C, E dan beta-karoten yang lebih tinggi meningkatkan jumlah berbagai subset sel T, meningkatkan respons limfosit terhadap mitogen, meningkatkan produksi IL-2 dan aktivitas sel NK, meningkatkan respons terhadap vaksin virus influenza, dan menyebabkan lebih sedikit hari infeksi. Suplementasi dengan formulasi mikronutrien kompleks pada orang tua meningkatkan jumlah berbagai jenis sel kekebalan, termasuk limfosit total, dan menyebabkan pergeseran dari sel T memori ke sel T naif. Suplementasi multi mikronutrien pada orang tua juga dapat mengurangi penggunaan antibiotik dan menyebabkan respon imun pasca vaksinasi yang lebih tinggi.
Kekurangan seng marjinal umum terjadi pada orang tua, karena asupan makanan mereka umumnya lebih rendah dan konsentrasi seng plasma menurun seiring bertambahnya usia, mungkin terkait dengan gangguan penyerapan, perubahan pengambilan sel, dan disregulasi epigenetik metilasi DNA atau jalur metionin / transsulfurasi, misalnya. Suplementasi dengan dosis rendah hingga sedang seng pada orang tua yang sehat dapat membantu memulihkan aktivitas timulin, meningkatkan jumlah sel T sitotoksik, mengurangi jumlah sel Th yang diaktifkan (yang berkontribusi pada autoimunitas) dan meningkatkan sitotoksisitas sel NK , manfaat imunologi yang membantu mengurangi kejadian infeksi seperti flu biasa, luka dingin dan influenza, serta insiden dan morbiditas pneumonia. Ada beberapa laporan bahwa pasokan seng yang cukup dapat mencegah penyakit terkait usia degeneratif termasuk infeksi dan kanker. Vitamin C yang cukup juga penting pada orang tua, yang berisiko kekurangan vitamin C, terutama wanita. Asupan vitamin C yang cukup dapat mengoptimalkan tingkat sel dan jaringan dan membantu melindungi dari infeksi pernapasan dan sistemik (misalnya, mengurangi durasi dan keparahan pneumonia), sedangkan tingkat yang lebih tinggi diperlukan selama infeksi untuk mengimbangi peningkatan respons inflamasi dan kebutuhan metabolik disebabkan oleh patogen, dan dengan demikian membantu mengurangi durasi dan keparahan gejala. Suplementasi dengan vitamin E pada orang tua telah terbukti secara signifikan meningkatkan aktivitas sitotoksik NK, kemotaksis neutrofil dan respon fagositik, dan meningkatkan proliferasi limfosit yang diinduksi mitogen dan produksi IL-2. Vitamin E juga dapat meningkatkan imunitas yang dimediasi oleh sel-T dan meningkatkan produksi antibodi sebagai respons terhadap vaksin hepatitis B dan tetanus. Risiko infeksi saluran pernapasan bagian atas, terutama flu biasa, secara signifikan lebih rendah setelah suplementasi vitamin E pada penghuni panti jompo, meskipun tidak ada efek yang jelas pada infeksi saluran pernapasan bagian bawah. Namun, tidak semua penelitian melaporkan efek menguntungkan pada infeksi saluran pernapasan dengan suplementasi vitamin E pada orang tua.
I.6. KESIMPULAN
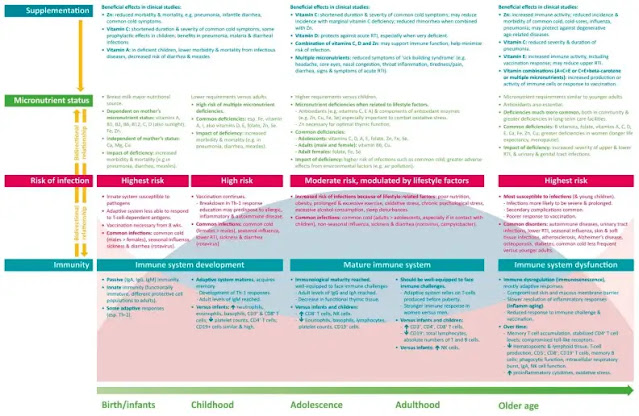
Sistem kekebalan mengalami banyak perubahan selama perjalanan hidup — berkembang dan menjadi dewasa selama masa kanak-kanak, berpotensi mencapai fungsi puncak pada awal masa dewasa, dan secara bertahap menurun pada kebanyakan orang di usia tua (sebagaimana gambar di bawah ). Ciri-ciri kekebalan yang berbeda hadir selama setiap tahap kehidupan, dan faktor-faktor spesifik secara berbeda memengaruhi fungsi kekebalan, dengan perbedaan yang dihasilkan dalam jenis, prevalensi, dan tingkat keparahan infeksi seiring bertambahnya usia. Faktor umum sepanjang hidup adalah kebutuhan akan pasokan mikronutrien yang cukup, yang memainkan peran kunci dalam mendukung fungsi kekebalan. Defisiensi mikronutrien multipel umum terjadi di seluruh dunia, dengan kemungkinan meningkat seiring bertambahnya usia. Suplementasi yang disesuaikan berdasarkan kebutuhan spesifik setiap kelompok usia dapat membantu memberikan dasar yang memadai untuk fungsi kekebalan yang optimal. Data klinis yang tersedia menunjukkan bahwa suplementasi mikronutrien dapat mengurangi risiko dan keparahan infeksi dan mendukung pemulihan yang lebih cepat. Namun,lebih banyak penelitian diperlukan tentang efek suplementasi mikronutrien pada fungsi kekebalan dan hasil klinis. Namun demikian, pengetahuan saat ini mengenai pentingnya mikronutrien dalam kekebalan, efek defisiensi mikronutrien pada risiko dan keparahan infeksi, dan prevalensi status mikronutrien yang tidak memadai di seluruh dunia membentuk dasar yang kuat untuk penggunaan suplemen multi mikronutrien yang ditargetkan untuk mendukung kekebalan. selama hidup seseorang.dan prevalensi di seluruh dunia dari status mikronutrien yang tidak memadai membentuk dasar yang kuat untuk penggunaan suplemen multi mikronutrien yang ditargetkan untuk mendukung kekebalan selama hidup seseorang.dan prevalensi di seluruh dunia dari status mikronutrien yang tidak memadai membentuk dasar yang kuat untuk penggunaan suplemen multi mikronutrien yang ditargetkan untuk mendukung kekebalan selama hidup seseorang.
Perbedaan imunitas dan nutrisi seumur hidup. Ca, kalsium; Cu, tembaga; Fe, besi; I, yodium; Ig, imunoglobulin; Mg, magnesium; NK, pembunuh alami; RTI, infeksi saluran pernapasan; Se, selenium; Th, sel pembantu T; Zn, seng.



.jpeg)




Tidak ada komentar:
Posting Komentar